Europi, el símbol és Eu, i el nombre atòmic és 63. Com a membre típic dels lantànids, l'europi sol tenir una valència de +3, però també és comuna una valència d'oxigen de +2. Hi ha menys compostos d'europi amb un estat de valència de +2. En comparació amb altres metalls pesants, l'europi no té efectes biològics significatius i és relativament no tòxic. La majoria de les aplicacions de l'europi utilitzen l'efecte de fosforescència dels compostos d'europi. L'europi és un dels elements menys abundants a l'univers; només n'hi ha uns 5 a l'univers × 10-8% de la substància és europi.
L'europi existeix a la monazita
El descobriment de l'europi
La història comença a finals del segle XIX: en aquella època, excel·lents científics van començar a omplir sistemàticament les vacants que quedaven a la taula periòdica de Mendeleev analitzant l'espectre d'emissió atòmica. Des del punt de vista actual, aquesta feina no és difícil i un estudiant de grau la pot completar; però en aquella època, els científics només disposaven d'instruments de baixa precisió i mostres difícils de purificar. Per tant, en tota la història del descobriment dels lantànids, tots els "quasi" descobridors van seguir fent afirmacions falses i discutint entre ells.
El 1885, Sir William Crookes va descobrir el primer senyal, però no gaire clar, de l'element 63: va observar una línia espectral vermella específica (609 nm) en una mostra de samari. Entre el 1892 i el 1893, el descobridor del gal·li, el samari i el disprosi, Paul émile LeCoq de Boisbaudran, va confirmar aquesta banda i va descobrir una altra banda verda (535 nm).
A continuació, el 1896, Eugène Anatole Demarçay va separar pacientment l'òxid de samari i va confirmar el descobriment d'un nou element de terres rares situat entre el samari i el gadolini. Va separar amb èxit aquest element el 1901, marcant el final del viatge de descobriment: "Espero anomenar aquest nou element europi, amb el símbol Eu i la massa atòmica d'aproximadament 151".
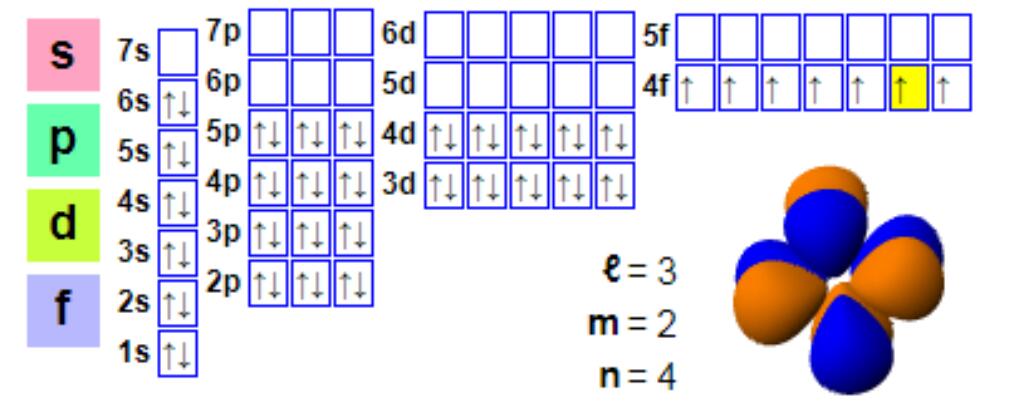
configuració electrònica
Configuració electrònica:
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p66s2 4f7
Tot i que l'europi sol ser trivalent, és propens a formar compostos divalents. Aquest fenomen és diferent de la formació de compostos de valència +3 per la majoria de lantànids. L'europi divalent té una configuració electrònica de 4f7, ja que la capa f semi-plena proporciona més estabilitat, i l'europi (II) i el bari (II) són similars. L'europi divalent és un agent reductor suau que s'oxida a l'aire per formar un compost d'europi (III). En condicions anaeròbiques, especialment en condicions de calefacció, l'europi divalent és prou estable i tendeix a incorporar-se al calci i altres minerals alcalinoterris. Aquest procés d'intercanvi iònic és la base de l'"anomalia negativa de l'europi", és a dir, en comparació amb l'abundància de condrita, molts minerals lantànids com la monazita tenen un baix contingut d'europi. En comparació amb la monazita, la bastnaesita sovint presenta menys anomalies negatives d'europi, de manera que la bastnaesita també és la principal font d'europi.
L'europi és un metall gris ferro amb un punt de fusió de 822 °C, un punt d'ebullició de 1597 °C i una densitat de 5,2434 g/cm³; És l'element menys dens, més tou i més volàtil entre els elements de terres rares. L'europi és el metall més actiu entre els elements de terres rares: a temperatura ambient, perd immediatament la seva brillantor metàl·lica a l'aire i s'oxida ràpidament en pols; reacciona violentament amb aigua freda per generar gas hidrogen; l'europi pot reaccionar amb bor, carboni, sofre, fòsfor, hidrogen, nitrogen, etc.
Aplicació de l'europi
El sulfat d'europi emet fluorescència vermella sota llum ultraviolada
Georges Urbain, un jove químic destacat, va heretar l'instrument d'espectroscòpia de Demarçay i va descobrir que una mostra d'òxid d'itri(III) dopada amb europi emetia llum vermella molt brillant el 1906. Aquest és el començament del llarg viatge dels materials fosforescents d'europi, que no només s'utilitzen per emetre llum vermella, sinó també llum blava, perquè l'espectre d'emissió de l'Eu2+ es troba dins d'aquest rang.
Un fòsfor compost d'emissors vermells Eu3+, verds Tb3+ i blaus Eu2+, o una combinació d'ells, pot convertir la llum ultraviolada en llum visible. Aquests materials tenen un paper important en diversos instruments arreu del món: pantalles intensificadores de raigs X, tubs de raigs catòdics o pantalles de plasma, així com en les recents làmpades fluorescents d'estalvi d'energia i els díodes emissors de llum.
L'efecte de fluorescència de l'europi trivalent també es pot sensibilitzar mitjançant molècules aromàtiques orgàniques, i aquests complexos es poden aplicar en diverses situacions que requereixen una alta sensibilitat, com ara tintes i codis de barres antifalsificació.
Des de la dècada del 1980, l'europi ha jugat un paper destacat en l'anàlisi biofarmacèutica d'alta sensibilitat mitjançant el mètode de fluorescència freda amb resolució temporal. A la majoria d'hospitals i laboratoris mèdics, aquesta anàlisi s'ha convertit en rutina. En la investigació de les ciències de la vida, inclosa la imatge biològica, les sondes biològiques fluorescents fetes d'europi i altres lantànids són omnipresents. Afortunadament, un quilogram d'europi és suficient per suportar aproximadament mil milions d'anàlisis: després que el govern xinès restringís recentment les exportacions de terres rares, els països industrialitzats espantats per l'escassetat d'emmagatzematge d'elements de terres rares no han de preocupar-se per amenaces similars a aquestes aplicacions.
L'òxid d'europi s'utilitza com a fòsfor d'emissió estimulada en un nou sistema de diagnòstic mèdic de raigs X. L'òxid d'europi també es pot utilitzar per fabricar lents de colors i filtres optoelectrònics, per a dispositius d'emmagatzematge de bombolles magnètiques i en materials de control, materials de blindatge i materials estructurals de reactors atòmics. Com que els seus àtoms poden absorbir més neutrons que qualsevol altre element, s'utilitza habitualment com a material per absorbir neutrons en reactors atòmics.
En el món actual, en ràpida expansió, l'aplicació recentment descoberta de l'europi pot tenir un impacte profund en l'agricultura. Els científics han descobert que els plàstics dopats amb europi divalent i coure univalent poden convertir eficaçment la part ultraviolada de la llum solar en llum visible. Aquest procés és força verd (és el color complementari del vermell). L'ús d'aquest tipus de plàstic per construir un hivernacle pot permetre a les plantes absorbir més llum visible i augmentar el rendiment dels cultius aproximadament en un 10%.
L'europi també es pot aplicar als xips de memòria quàntica, que poden emmagatzemar informació de manera fiable durant diversos dies. Aquests poden permetre que les dades quàntiques sensibles s'emmagatzemin en un dispositiu similar a un disc dur i s'enviïn a tot el país.
Data de publicació: 27 de juny de 2023